BEGOの虚偽(ごまかし)のリスク分析
2019年8月16日
一般財団法人電気安全環境研究所(JET)
製品認証部 医療機器認証室 W 様
いつも大変お世話になっています。
1. BEGOの歯科鋳造用コバルト・クロム合金 (クラスⅡ)のリスク分析は、歯科陶材焼付用ニッケル・クロム合金のリスク分析内容であることを、BEGOの提出したリスク分析の記載部分を明示して、私は2013年12月16日に、JETのI様とN様にお送り致しました。
その日から6年になります。もう一度、その書面をご覧になって下さい。
ここで再度、その一部をご説明させて頂きます。

(ⅰ)
リスク分析表(Ⅰ)の赤枠内の赤線※が品目名です。ウイロニウム プラスと書かれています。
ウイロニウム プラスは歯科鋳造用コバルト・クロム合金です。
しかし、ここに書かれているのは歯科陶材焼付用ニッケル・クロム合金のリスク分析です。
(ⅱ)
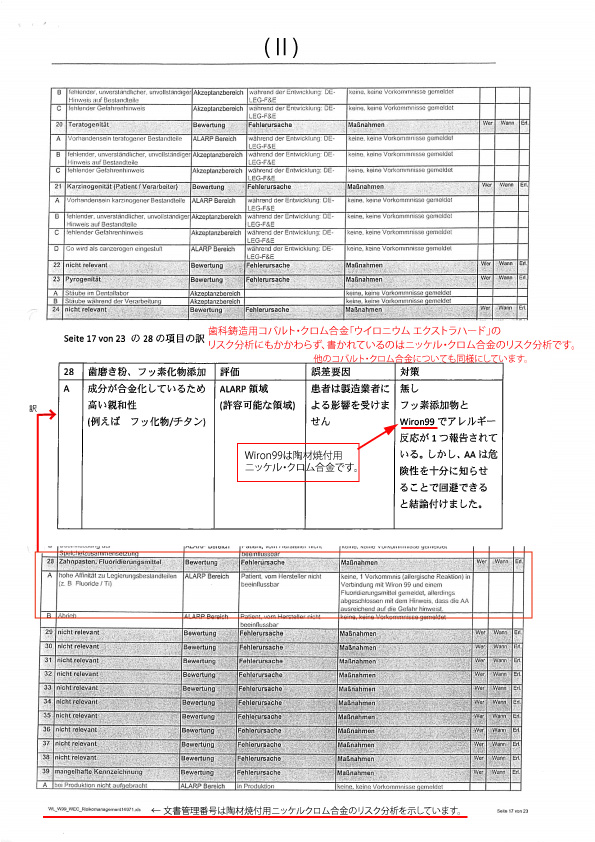
リスク分析表(Ⅱ)はウイロニウム EHのリスク分析です。
ウイロニウム EHは鋳造用コバルト・クロム合金です。
しかし、リスク分析表(Ⅱ)の28 Aの欄にはニッケル・クロム合金についてのリスク分析が書かれています。

(ⅲ)
リスク分析表(Ⅲ)は ウイロニット LAのリスク分析です。 ウイロニット LAは鋳造用コバルト・クロム合金です。
しかし、ここに書かれているのは、ニッケル・クロム合金のリスク分析です。
(Ⅲ)の赤枠内を訳します。
8. 残留リスク総合評価
ウイロン ライト/ ウイロン 99 / ウイロセル プラスは、歯科陶材焼付用合金に関するISO 9693およびISO 22674のすべての要件を満たしています。
in vitroの腐食性試験は、成分の溶出が非常に低いので全身毒性効果はないことを示唆しています。
ISO10993-1に従って独立機関(Dr.Henning&Co. Dental Engineering / Basle)により感作性試験が細胞で試験され、その結果、細胞毒性および感作性のないことが認証されました。
歯科用ニッケルの高いアレルギー誘発性から特定の残存リスクがあります。ドイツでは女性の最大20%、男性の8%がニッケルにアレルギーがあると考えられています。
歯科用のニッケル・クロム合金がニッケルアレルギーを引き起こすことは、ごく少数の事例についてのみ文書化されています。
ウイロン ライト /ウイロン99 / ウイロセル プラスに類似した合金の成分の割合では、これらの文書化されたケースの中でさらに非常に低くなっています。
BEGOは、数十年にわたってそのような合金(ウイロン77、ウイロン88)を販売しています。
BfArMには、フッ素化剤の存在下でのウイロン 99に対するアレルギー反応の疑いがあります(ケース番号:4345)。 BfArMは、ウイロン99の製品情報が、アレルギー反応の可能性を十分に示していると言って、この訴訟を暫定的にクローズしました。
全体的なリスク評価は、今日の観点から正しいと判断できます。
このリスク評価に基づくさらなる対策は必要ないと思われます。 リスク管理レポートは以下によって作成されました。
DrA、DrSt、Gr ブレーメン
DrA署名による印刷
この文書管理番号はWL_W99_WEC_Risikomanagement14971.xls となっていて、歯科陶材焼付用ニッケル・クロム合金「ウイロンライト、ウイロン99、ウイロセル」のリスク分析文書であることがわかります。
BEGOは、このニッケル・クロム合金のリスク分析の製品名を歯科鋳造用コバルト・クロム合金の「ウイロニット LA」に書き換えてJETに提出し、JETはそれを受理しています。
JETは、このようなBEGOの虚偽のリスク分析を受理し、BEGO Dental(株式会社ニッシン)のために認証したことは間違いです。
2. ウイロニットLAに関して
JETがBEGOに推薦した薬事コンサルタントの山本款路氏は、弊社の旧承認書のウイロニットLAの成分:Co 63.5%, Cr 29%, Si 1.2%
をCo 64.0%, Cr 28.5%, Si 0.5%に変えて申請し、JETはそれを認証しました。
なぜ、弊社の旧承認書の成分を改ざんして、それを類似医療機器として本来の弊社の旧承認書の成分を新規製品として認証されましたか。
弊社の旧承認書の内容を改ざんして申請したものを認証したことは間違いです。
3. 厚生労働省医薬食品局 審査管理課医療機器審査管理室
「改正薬事法のポイント ~承認・認証制度及び販売規制~」
(Ⅳ) (医療機器)新独法の安全情報によるリスクマネジメント

(医療機器)新独法の安全情報によるリスクマネジメント(Ⅳ)をご覧下さい。
説明図によりますと、市販後問題が起れば、リスクの再検討・評価のためリスク分析を再び行う流れになっています。
JETは、弊社の申請途中から申請者をBEGOに変更し、弊社にはリスク分析の内容を知らせませんでした。
弊社は、後日、山本款路氏から申請書控えとして買わされ、その後リスク分析の内容を知りました。
BEGOの鋳造用コバルト・クロム合金のリスク分析は、陶材焼付用ニッケル・クロム合金のリスク分析内容で品目名のみ鋳造用コバルト・クロム合金に書き換えた、ごまかしの書面です。
リスク分析ができていない製品を認証するために、なぜ弊社のCEOを生物学的安全性評価者にしましたか。
旧法下の弊社旧承認書の内容をBEGOのコンサルタント山本款路氏とJETが改ざんして、BEGOの虚偽のリスク分析を担保するために弊社のCEOを生物学的安全性評価者にし、そのまま放置していることは間違いです。
JETが作成した、BEGOのDistribution AgreementのANNEX Ⅶ (GQP契約)を正式に解除して下さい。
そして、弊社CEOのみならずCEO家族も心身共に傷つき苦しんでいます。
先ず、弊社にいらして下さり、弊社全員がどれほど切り詰めた生活をし、貧しさの極みに達しているかを、ご自身の目で確かめて下さい。
きっと弊社の苦しみが、直ちにおわかりになります。
一日も早く、ご来社下さいますように、お祈り致します。
エーピーエス株式会社
取締役 中井陽子